肾脏是糖尿病微血管损伤的重要靶器官。相当大比例的糖尿病患者会因其疾病和/或其他并发症而患上肾脏疾病。越来越多的证据表明肾小球内皮(glomerular endothelial cells,GECs)损伤在糖尿病肾病(diabetic kidney disease,DKD)中起主要作用,DKD的严重程度与2型糖尿病的内皮功能障碍正相关。DKD进展可能与患者血浆中内皮细胞衍生的血管性血友病因子、可溶性血管细胞粘附分子-1和可溶性细胞间粘附分子-1水平升高,糖萼减少、内皮细胞凋亡有关。然而,内皮损伤在DKD发病机制中的作用尚不清楚。线粒体功能障碍与DKD的发生发展密切相关。目前靶向线粒体功能障碍的新疗法成为研究热点,以预防或治疗DKD。在DKD的实验模型中,有研究者使用电子显微镜观察到肾内皮细胞线粒体结构异常。有趣的是,线粒体功能障碍的标志物8-oxoG仅在CD31阳性的GECs中可检测到,在中度至重度或晚期DKD组织病理学病例受试者的足细胞中并未检测到8-oxoG。因此,针对GECs的线粒体内稳态可能是预防或改善DKD的一种有希望的新治疗策略。

2022年10月18日,温州医科大学李校堃院士团队在Diabetes上发表了题为“FGF13-sensitive alteration of Parkin safeguards mitochondrial homeostasis in endothelium of diabetic nephropathy”的研究论文。该研究发现非分泌性生长因子FGF13可通过对Parkin的动态调控监管GECs的线粒体稳态环节,从而参与调控DKD。beat365亚洲版官网丛维涛研究员,金利泰教授为论文并列通讯作者,beat365亚洲版官网博士研究生孙佳,附属第二医院心内科官学强主任为论文共同第一作者。
经典分泌型FGF信号在DKD病理发展中的重要角色已被广泛证明。在此方面,内分泌FGF亚家族的成员FGF21,其表达受脂肪组织中的PPARc调节,在啮齿类动物中是一种有效的降糖剂。此外,FGF蛋白家族的原型—aFGF,最近被发现可通过抑制受损肾组织中的炎症信号级联效应来改善DKD。然而,关于非分泌性蛋白FHF亚家族在DKD中的功能知之甚少。FGF13是非分泌性蛋白FHF家族的一员,其在神经元发育、痛觉及氧觉调控、心脏生理及病理学调控等方面的作用近年来受到越来越多的关注。然而,迄今为止,有关FGF13在肾脏疾病中的作用受到较少关注。随着DKD的病程发展,FGF13在肾脏内皮细胞中被诱导高表达。而内皮细胞特异性敲除Fgf13则缓解了DKD进展,Fgf13基因的过表达表现出相反的趋势。转录组测序分析提示线粒体稳态参与了FGF13对于DKD的调控。
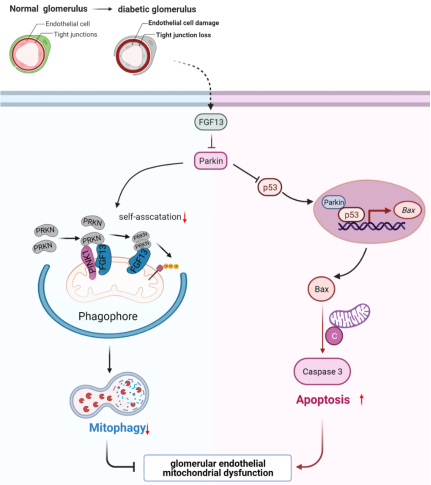
此外,李校堃院士团队发现Parkin是糖尿病条件下FGF13发挥线粒体稳态调控效应的重要作用靶点。Parkin是线粒体质量控制的关键调节因子,在线粒体损伤时参与决定细胞命运。研究人员进一步考察了FGF13调节Parkin的机制,并发现FGF13通过Parkin介导GECs中对线粒体自噬和凋亡的调节在机制上是不同的。FGF13可通过抑制Parkin的self-association环节来调节Parkin依赖性的线粒体自噬;Parkin-p53-Bax信号轴参与了DKD条件下FGF13介导的细胞凋亡。
综上所述,本研究发现Fgf13缺失在通过Parkin介导抑制凋亡和促进线粒体自噬中的双重作用可显著促进GECs中的线粒体稳态这一关键环节,从而缓解DKD进程。FGF13可作为预防和控制T2DN的靶点,并为其他与FGF13和Parkin相关疾病发病机制的研究提供新思路。
原文链接:https://diabetesjournals.org/diabetes/article-abstract/doi/10.2337/db22-0231